Pfizer čoskoro požiada úrady o schválenie 3. dávky vakcíny proti covidu pre deti
Konzorcium spoločností Pfizer a BioNTech vo štvrtok oznámilo pozitívne výsledky klinických skúšok, týkajúcich sa bezpečnosti a imunitnej reakcie na tretiu dávku jeho vakcíny proti koronavírusu u detí vo veku päť až 11 rokov. Spoločnosti dodali, že čoskoro požiadajú regulačné úrady o schválenie.
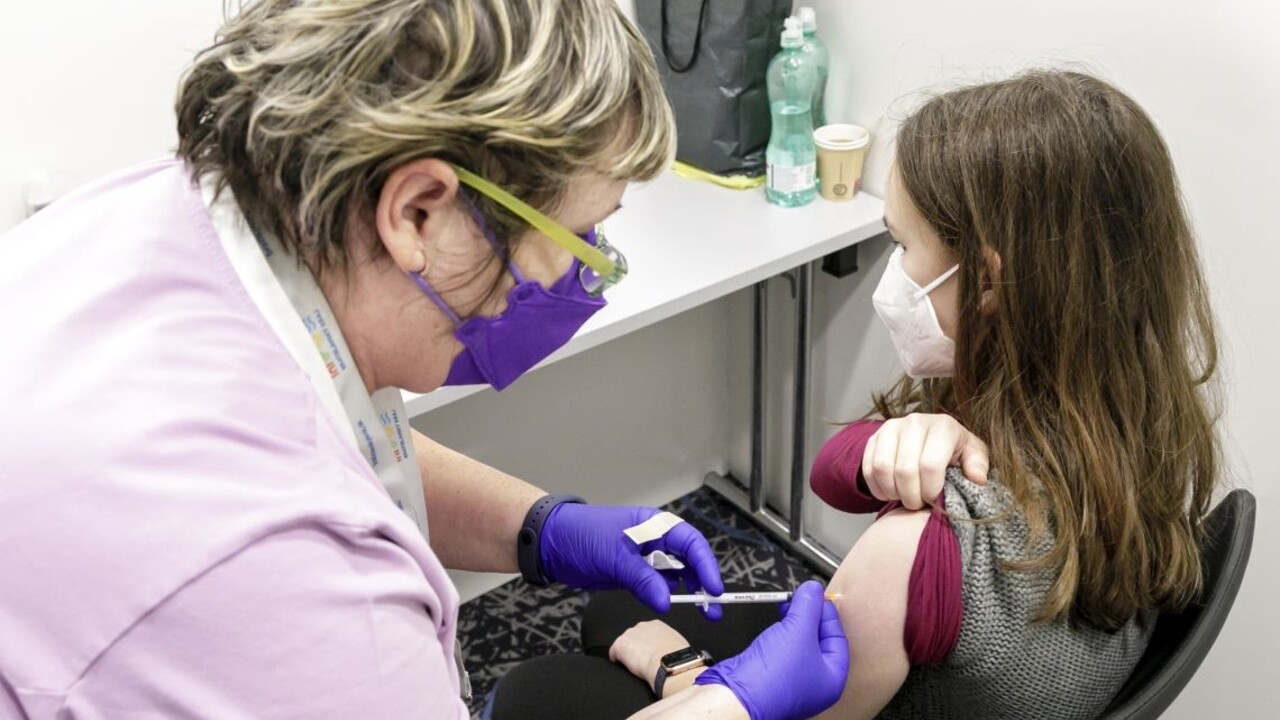
Tretia dávka vakcíny je už odporúčaná pre ľudí vo veku 12 rokov a viac; štvrtá dávka bola nedávno odporučená pre ľudí nad 50 rokov. Mladšie deti - s výnimkou tých, ktoré majú poškodenú imunitu (trpia imunosupresiou) - nie sú oprávnené dostať tretiu dávku, preto sú náchylnejšie na nákazu variantom koronavírusu omikron a jeho subvariantom BA.2, pripomína AFP.
BA.2 je v súčasnosti celosvetovo prevládajúcim subvariantom a pripisuje sa mu aj terajší prudký nárast v prípadoch infekcie na severovýchode Spojených štátov. Spoločnosti Pfizer a BioNTech vo fáze skúšky 2/3 analyzovali údaje od 140 detí vo veku päť až 11 rokov, približne šesť mesiacov po druhej dávke.
Dávka v tejto vekovej skupine je desať mikrogramov a bola zvolená z bezpečnostných dôvodov, keďže deti sú náchylnejšie na vedľajšie účinky vakcíny. Dávka pre deti vo veku 12 a viac rokov je 30 mikrogramov. Pri analýze údajov od 140 detí sa zistilo, že tieto osoby tretiu dávku znášali dobre a neboli odhalené žiadne nové zdravotné riziká.
Pfizer a BioNTech plánujú tieto údaje čoskoro odovzdať americkému Úradu pre kontrolu potravín a liečiv (FDA), Európskej agentúre pre lieky (EMA) a ďalším regulačným orgánom. Väčšina krajín, vrátane USA, ešte vakcíny proti covidu pre dojčatá a veľmi malé deti neschválila, pripomína AFP. Minulý mesiac spoločnosť Moderna oznámila, že požiadala o schválenie svojej vakcíny pre deti vo veku šesť mesiacov až päť rokov, pričom režim má byť dvojdávkový.


